Co víme o vodě
03. 03. 2026
Události Svět
Molekula vody je poměrně jednoduchá, vyznačuje se však řadou překvapivých vlastností.
Zásoby vody na Zemi se odhadují na 1,5 mld. km3. Drtivou většinu z toho (95 %) tvoří slaná voda v oceánech. Přibližně 3 % světových zásob vody se nacházejí ve formě vody podzemní, přičemž zhruba dvě třetiny jsou rovněž slané. Sladkou vodu najdeme kromě podzemí zejména v ledovcích (1,7 %) a pouze méně než 0,2 % zbývají na sladkou vodu povrchovou a atmosférickou.
Z celkového povrchu Země 510 mil. km2 pokrývají oceány a moře 360,7 mil. km2 (70,7 %) a pevnina 149,3 mil. km2 (29,3 %). Na mapě pevniny bychom naměřili asi 4 mil. km2 jezer, rybníků a vodních nádrží a 0,77 mil. km2 řek.
Voda na planetě Zemi
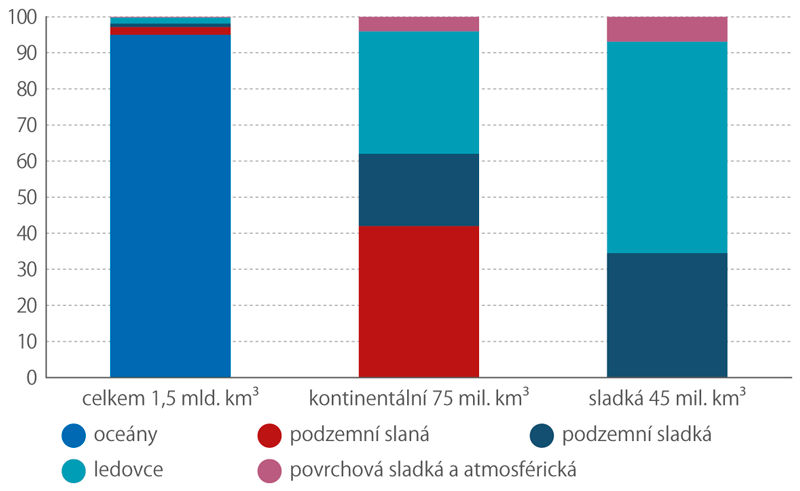
Zdroj: NASA – Surface Water and Ocean Topography
Vodní anomálie
Voda má mnoho zajímavých fyzikálních a chemických vlastností. Její molekula se skládá z jednoho atomu kyslíku a dvou atomů vodíku, přičemž vodíky jsou na kyslík navázané nikoliv symetricky naproti sobě, ale v úhlu 105°. Kyslík zároveň od vodíku přetahuje na svou stranu elektrony, takže navenek je kyslík zdrojem záporného náboje a vodík kladného. To mj. způsobuje, že molekuly vody jsou k sobě přitahovány tzv. vodíkovými můstky, které jsou zase jednou z příčin tzv. tepelné roztažnosti vody. Drtivá většina látek se vzrůstající
teplotou zvyšuje svůj objem. Při zahřívání lihu, rtuti, ale také většiny pevných látek a plynů se tyto látky roztahují a při ochlazování zase smršťují. To se v případě vody děje stejně, ovšem s výjimkou teplotního rozmezí od 0 do 3,8 °C. V tomto intervalu se při zahřívání hustota vody zvyšuje (objem se tedy zmenšuje), ochlazováním naopak klesá hustota a zvětšuje se objem. V zimě, působí-li na hladinu rybníka mráz, voda se ochladí na 3,8 °C a klesne ke dnu, protože má nejvyšší hustotu. Pokud ochlazování pokračuje, chladnější voda již zůstává nahoře, kde se změní v led. Ten, jelikož je lehčí než kapalná voda, plave a vytvoří příkrov nad tekutou vodou pod sebou, v níž mohou přežívat ryby a další vodní živočichové.
Další dvě fyzikální vlastnosti brání tomu, aby vodní nádrže promrzaly příliš rychle a v led se během zimy proměnila veškerá jejich voda. Nízká tepelná vodivost způsobuje, že teplo prostupuje vodou velmi pomalu. Než tedy energie z teplejšího dna vystoupá ke studenějšímu povrchu, trvá to poměrně dlouho. Naproti tomu vysoká měrná tepelná kapacita znamená, že k ohřátí jednoho litru vody potřebujeme poměrně velké množství energie. To platí i opačně: k ochlazení je třeba velké množství energie odebrat. Je-li nádrž dostatečně hluboká, nestihne voda v průběhu chladného období odevzdat všechno naakumulované teplo do vzduchu a ve spodních vrstvách se udrží velmi dlouhou dobu v tekutém stavu.
Mezi další mimořádně vlastnosti vody patří vysoké povrchové napětí. Vlivem tohoto fyzikálního jevu se na hladině tvoří tenká poměrně pevná vrstvička, která například umožňuje některým druhům hmyzu (vodoměrky, bruslařky) chodit po vodě. Povrchovému napětí vděčí také vodní ptáci za to, že se jejich peří nepromáčí. Z běžně dostupných látek mají vyšší povrchové napětí než voda pouze rtuť a koncentrované cukerné roztoky, případně velmi slaná voda.
Na vlastnostech vody je založena i světově nejrozšířenější teplotní stupnice, kterou v roce 1742 vytvořil švédský fyzik Anders Celsius. Stupnice přiřazuje hodnotu 0 °C teplotě tuhnutí vody a 100 °C teplotě varu. Celsius měl původně pořadí obráceně. Varu odpovídala nula a tuhnutí stovka. Do současné podoby stupnici otočil v roce 1745 Carl Linné.
Není voda jako voda
Standardní molekula vody obsahuje vodík, jehož atomová jádra jsou tvořena pouze protonem. V některých molekulách má však vodík ve svém jádře kromě protonu také neutron. Takový vodík má oproti běžnému dvojnásobnou hmotnost a označuje se jako deuterium. Voda z něho nese název těžká voda. V přírodě je těžká voda přirozenou součástí normální vody, vyskytuje se v ní však pouze ve stopovém množství. Od běžné vody se odlišuje některými fyzikálními vlastnostmi a lidé ji využívají například při řízení štěpných reakcí v jaderných reaktorech. Deuterium izolované z těžké vody by také v budoucnu mělo sloužit jako hlavní palivo v zařízeních využívajících termojadernou fúzi, tedy přeměnu vodíku na helium.
Další zajímavou variantou je tzv. kovová voda. Jedná se o vodu, která se chová jako kov a měla by být přítomna v jádrech velkých planet. Vzhledem k velmi vysokému tlaku potřebnému k jejímu vzniku se až do nedávna předpokládalo, že v pozemských podmínkách ji nelze získat. Týmu vědců pod vedením Pavla Jungwirtha z Akademie věd ČR se však v roce 2021 podařilo uskutečnit experiment, při kterém kovovou vodu vyrobili bez nutnosti využívat extrémní tlak. Na rozdíl od těžké vody nemá kovová voda zatím žádné praktické využití, nicméně metoda jejího získávání se může uplatnit při výrobě jiných materiálů.
V lékařství a kosmetice se používá borová voda, která je slabým roztokem kyseliny borité (H3BO3). V nízké koncentraci má dezinfekční účinky a pomáhá např. při léčbě zánětů očí nebo uší. Dříve se kyselina boritá přidávala i jako konzervant do potravin, Evropská agentura pro chemické látky (ECHA) ji však zařadila na seznam látek vzbuzujících mimořádné obavy, a proto se již v potravinářství (až na výjimky) nepoužívá.
Za zmínku ještě stojí kalná voda v přírodních nádržích, ale i v řekách po intenzivním dešti. Ta bývá příčinou mnoha tragédií, kdy lidé podcení riziko a do takové vody se vydají koupat. V kalné vodě snadno narazíme na překážku, o níž jsme netušili a která nás může porazit, stáhnout nebo jen narušit naši rovnováhu. To stačí, abychom ve zmatku trochu vody vdechli a začali se topit. Tonoucí oproti vžité představě nekřičí, protože se nemůže nadechnout, ani zpravidla divoce nemáchá rukama. Obvykle po několika cukavých pohybech tiše zmizí pod hladinou. Pokud je voda zakalená, ztratí se ostatním z očí a najít jeho tělo včas, bývá prakticky nemožné.
Počty utonulých v Česku
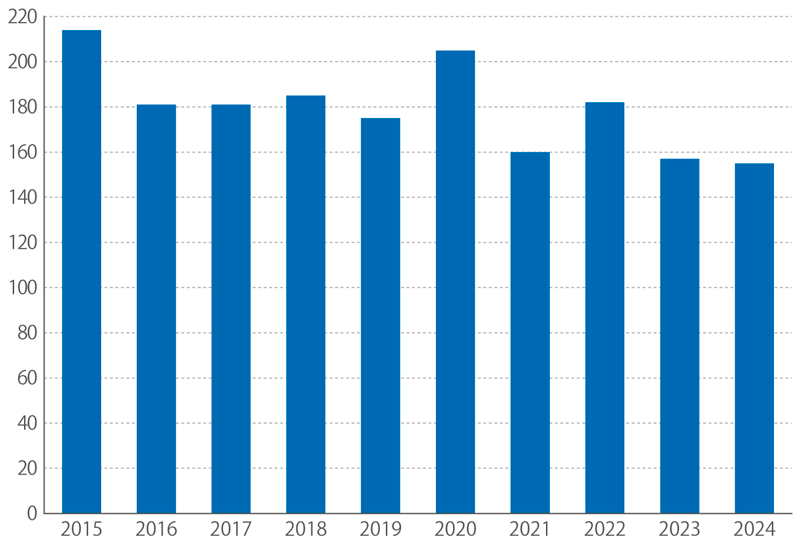
Zdroj: ČSÚ
Voda ve vesmíru
Odhadnout množství vody na tělesech sluneční soustavy se ve své práci pokusil planetolog z Jet Propulsion Laboratory NASA Steve Vance. Podle jeho výpočtů se nejvíce této tekutiny nachází na největším Jupiterově měsíci Ganymedes. Voda tvoří více než dvě třetiny objemu Ganymeda a jenom v kapalném stavu by jí zde mělo být sedmadvacetkrát víc než na Zemi. Druhý v pořadí je Saturnův měsíc Titan. Množství kapalné vody na něm přesahuje objem zemské vody čtrnáctkrát a celkově se na jeho objemu voda podílí 44 %.
I další tělesa Sluneční soustavy jsou na vodu poměrně bohatá, Země se s pouhými 0,12 % vody ve svém složení řadí do velmi „suché“ části žebříčku. Podle některých teorií má většina pozemské vody svůj původ v kometách, které se s naší planetou kdysi srazily. Dnes jsou zbylé komety soustředěny v tzv. Oortově oblaku, nacházejícím se ve vzdálenosti asi 50 000 astronomických jednotek od Slunce.
Zatím největší zásobárna vody ve vesmíru byla objevena v galaxii APM 08279+5255 vzdálené od nás více než 12 miliard světelných let. Podle pozorování spektrometrem na havajské Caltech Submillimeter Observatory přesahuje hmotnost vody v ní obsažené stotisíckrát hmotnost našeho Slunce.
Podíl vody na objemu vybraných těles sluneční soustavy
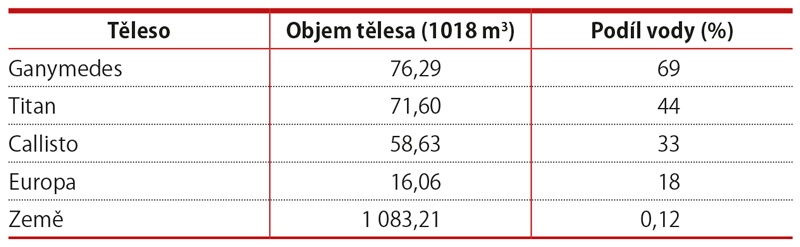
Zdroj: Steve Vance, NASA
